Contoh Soal Fraksi Mol – Mata pelajaran Kimia pastinya sudah mulai diperkenalkan sejak duduk di bangku SMP (Sekolah Menengah Pertama). Kemudian di jenjang SMA atau SMK, materi tentang Kimia mulai berkembang.
Nah, khusus untuk kalian yang sudah duduk di bangku SMA atau SMK dari kelas 10 sampai 12, nantinya kalian akan menerima pembahasan materi Kimia tentang Fraksi Mol. Materi bisa dibilang cukup sulit, karena ada rumus perhitungan seperti di mata pelajaran Fisika.
Oleh karena itu, melalui artikel berikut kami akan mengajak kalian untuk belajar lebih jauh soal materi Fraksi Mol. Disini kami telah menyiapkan beberapa contoh soal lengkap dengan pembahasan dan jawabannya.
Bukan hanya itu, kalian juga bisa belajar bagaimana cara menghitung Fraksi Mol menggunakan rumus yang tersedia. Baiklah, supaya lebih jelas langsung saja simak contoh soal Fraksi Mol untuk kelas 11 dan 12 SMA dibawah ini.
Pengertian Fraksi Mol
Di dalam mata pelajaran Kimia, pasti banyak dari kalian yang sudah tahu kalau konsentrasi larutan berhubungan erat dengan zat pelarut maupun zat terlarut. Kemudian proses penyatuan hubungan zat pelarut dan terlarut disebut dengan Fraksi Mol.
Dengan begitu, Fraksi Mol bisa dikatakan sebagai satuan konsentrasi antara jumlah mol zat terlarut atau pelarut pada jumlah mol larutan (mol Pelarut + mol Terlarut). Materi Kimia mengenai Fraksi Mol kerap muncul di soal-soal Ulangan harian, Ujian Semester dan Ujian Sekolah.
Jadi selain mempelajari contoh soal tekanan zat padat, molekul dan Ide Laju Reaksi,kalian juga perlu mempelajari contoh soal Fraksi Mol.
Rumus Menghitung Fraksi Mol
Nantinya dalam mengerjakan soal Fraksi Mol kalian tentu harus mengetahui rumus yang dibutuhkan. Dalam menentukan rumus saat menghitung Fraksi Mol disesuaikan dengan jenis Fraksi Mol itu sendiri.
Ada dua jenis Fraksi Mol, yaitu Zat Xt dan Zat Xp, masing-masing jenis Fraksi Mol memiliki ketentuan rumus yang berbeda-beda. Informasi selengkapnya bisa kalian simak dibawah ini :
1. Mol Zat Pelarut (Xt)
Pertama, untuk jenis Fraksi Mol Zat Pelarut (Xt) kalian bisa menggunakan rumus :
Xt + Xp = 1
2. Mol Zat Terlarut (Xp)
Sedangkan untuk Fraksi Mol Zat Terlarut (Xp) rumus yang digunakan adalah :
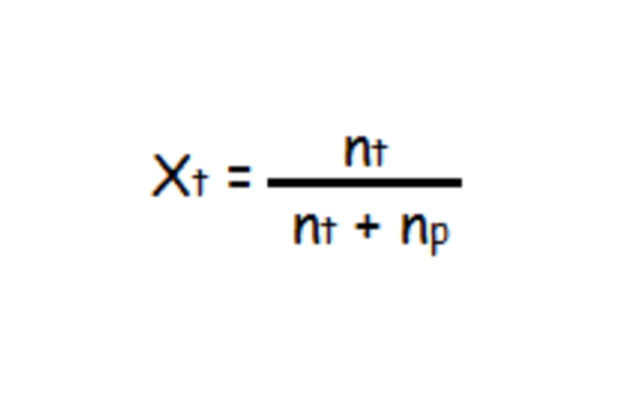
Xt = Fraksi mol zat terlarut
Np = Jumlah mol zat pelarut
Nt = Jumlah mol zat terlarut
Contoh Soal Fraksi Mol

Sampai disini kalian sudah tahu seperti apa rumus menghitung soal Fraksi Mol, baik itu Fraksi Mol Xt Maupun Fraksi Mol Xp. Selanjutnya, kami bakal menyajikan beberapa contoh soal Kimia kelas 10 sampai kelas 12 SMA untuk materi Fraksi Mol.
Pada contoh soal yang akan kami sajikan berikut ini sudah dilengkapi dengan jawaban dan pembahasan dari masing-masing contoh soal. Dengan begitu, kalian bisa memakai contoh soal berikut sebagai pembelajaran agar ketika menemukan soal Fraksi Mol bisa mudah menyelesaikannya.
Contoh Soal 1
Solusinya terdiri dari 3 mol zat A, 3 mol zat B dan 4 mol zat C. Bagaimanakah menghitung fraksi mol?
Diketahui :
- nA = 3
- nB = 3
- nC = 4
Jawaban :
XA = nA / (nA + nB +nC)
XA = 3 / (3 + 3 + 4)
XA = 0.3
XA = nA / (nA + nB +nC)
XA = 3 / (3 + 3 + 4)
XA = 0.3
XA = nA / (nA + nB +nC)
XA = 4 / (3 + 3 + 4)
XA = 0.4
Jadi jumlah XA + XB + XC = 0.3 + 0.3 + 0.4 = 1
Contoh Soal 2
Jika ada sebuah larutan yang terdiri dari 2 mol zat A, 3 mol zat B, dan 5 mol zat C. Coba hitung masing-masing fraksi mol dari zat tersebut ?
Diketahui :
nA = 2
nB = 3
nC = 5
Jawaban :

Contoh Soal 3
Coba hitung dengan benar Fraksi mol urea 10% (Mr = 60) dalam pelarut air murni jika 100 gram larutan mengandung 10 gram urea
A. 0,032
B. 0,034
C. 3,2
D. 3,4
E. 0,32
Diketahui :
Massa larutan = massa terlarut + massa pelarut
100 gram = 10 gram + massa pelarut
massa pelarut = 100 gram – 10 gram
massa pelarut = 90 gram
Jawaban :

Contoh Soal 4
Jika terdapat 27,6 gram etanol C2H5OH yang dilarutkan dalam 54 gram H2O (Ar C = 12, H = 1, O = 16). Berapakah jumlah Fraksi Mol Etanol dan Fraksi Mol Air nya ?
Diketahui :

Jawaban :

Contoh Soal 5
Coba hitung berapa nilai fraksi mol etanol (Mr = 46) dari larutan etanol 46% massa!

Contoh Soal 6
Berapa Fraksi mol larutan 36 gram glukosa (Mr = 180) dalam 90 gram air (Mr = 18) ?
A. 0,960
B. 0,400
C. 0,040
D. 0,038
E. 0,004

Contoh Soal 7
Hitunglah berapa banyak etanol di dalam 800 ml larutan etanol 30% volume
Diketahui :
Volume larutan = 800 ml
% V = volume zat terlarut x 100%
volume larutan
Jawaban :
Volume zat terlarut = % V x volume larutan
100%
Volume etanol = 30 x 800 = 240 ml
100
KESIMPULAN
Itu saja ulasan dari Inspired2Write.com mengenai contoh soal dari materi Fraksi Mol untuk kelas 10, 11 dan 12 SMA / SMK. Diatas kami juga menjelaskan sedikit mengenai pengertian Fraksi Mol hingga cara menghitung Fraksi Mol menggunakan rumus yang berlaku. Semoga adanya contoh soal diatas bisa membantu kalian para siswa SMA maupun SMK dalam mengerjakan soal-soal Kimia ketika Ulangan harian, Ujian Semester dan Ujian Sekolah.
sumber gambar :
- ruangguru.co
- kontensekolah.com
- soalfismat.com
- kompas.com
