Contoh Soal Isokhorik – Termodinamika merupakan salah satu cabang ilmu fisika yang mempelajari proses perpindahan energi sebagai kalor dan usaha antara sistem dan lingkungan. Proses termodinamika adalah perubahan keadaan gas yaitu tekanan, volume dan suhunya.
Perubahan tersebut diiringi dengan perubahan kalor, usaha dan energi di dalamnya. Dalam teori hukum termodinamika, proses termodinamika meliputi beberapa proses yang memiliki sifat khusus, dimana yang akan dibahas kali ini adalah tentang proses isokhorik termodinamika.
Proses isokhorik terjadi pada tekanan tetap, dimana sistem tidak mengalami perubahan volume, meskipun sejumlah kalor memasuki atau keluar sistem. Dengan kata lain, usaha yang dilakukan sistem atau yang dilakukan lingkungan pada sistem adalah sama dengan nol (W = 0).
Nah, untuk lebih memahami dan mendalami lagi terkait proses isokhorik, berikut ini akan kami jelaskan rangkuman materi dan beberapa contoh soal isokhorik. Adapun bagi kalian yang ingin lebih menguasai teori termodinamika, maka silahkan simak ulasan lengkap di bawah ini.
Proses Isokhorik Dalam Termodinamika
Hukum yang menjelaskan perilaku gas pada volume tetap adalah Hukum Gay Lussac. Menurut hukum Gay Lussac, jika volume dijaga konstan, maka tekanan gas akan berbanding lurus dengan suhu gas. Keadaan gas jika volumenya dibuat tetap disebut keadaan isokhorik.
Sementara proses perubahan sistem pada volume tetap disebut proses isokhorik. Pada proses isokhorik, sistem tidak mengalami perubahan volume, walaupun sejumlah kalor masuk atau keluar sistem. Ini memberikan pengertian bahwa sistem tidak melakukan atau menerima usaha.
Dengan kata lain, usaha yang dilakukan sistem atau yang dilakukan lingkungan pada sistem sama dengan nol (W = 0). Jadi, dalam proses isokhorik berlaku persamaan :
W = 0 dan ΔU = Q
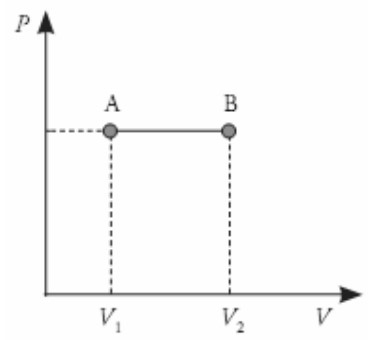
Contoh Soal Isokhorik

Nah, setelah mencermati rangkuman tentang proses isokhorik, selanjutnya untuk memahami lebih dalam lagi kalian bisa mencoba mencermati contoh soalnya. Seperti halnya contoh soal hukum Charles, berikut ini juga kami sajikan contoh soal isokhorik beserta pembahasannya.
Contoh Soal 1
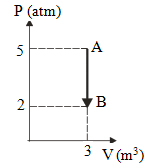 Gambar di atas menujukan, grafik tekanan (P) terhadap volume (V) dari suatu gas yang mengalami proses isokhorik. Usaha yang dilakukan gas pada proses AB yaitu …. Pembahasan : Proses AB ⇒ proses isokhorik (volume tetap). Pada volume isokhorik, volume gas tidak mengalami perubahan, sehingga tidak ada usaha yang dilakukan oleh AB (gas). |
Contoh Soal 2
| 0,2 mol gas monoatomik bersuhu 27°C berada di dalam sebuah bejana tertutup. Kalor yang harusnya masuk agar suhu gas bertambah menjadi 400 K adalah …. Jika diketahui konstanta gas umum (R) = 8,315 J/mol.K. Pembahasan : → Diketahui : Jumlah mol (n) = 0,2 mol Suhu awal (T1) = 27°C + 273 = 300 Kelvin Suhu akhir (T2) = 400 K Konstanta gas umum (R) = 8,315 J/mol.K → Ditanya : Kalor yang diserap (Q) ….? → Jawab : Pada proses isokhorik, gas tidak mengalami perubahan volume, sehingga tidak ada usaha yang dilakukan (W = 0) Hukum I Termodinamika : ΔU = Q – W ΔU = Q – 0 ΔU = Q Kalor yang diserap (Q) = pertambahan energi dalam gas (U). Perubahan energi dalam gas dihitung dengan rumus energi seperti dibawah ini. Energi dalam gas : ΔU = 3/2 nR ΔT = 3/2 nR (T2 – T1) ΔU = 3/2 (0,2)(8,315)(400 – 300) ΔU = 3/2 (0,2)(8,315)(100) ΔU = 249,45 Joule Jadi, kalor yang diserap oleh gas = perubahan energi dalam gas yaitu 249,45 Joule |
Contoh Soal 3
| Dalam sebuah bejana tertutup, terdapat gas yang semulanya bersuhu 27°C. Agar tekanan gas menjadi 2 kali lipat dari semula, maka suhu bejana tersebut adalah …. Pembahasan : → Diketahui : Tekanan awal (P1) = P Tekanan akhir (P2) = 2P Suhu awal (T1) = 27°C + 273 = 300 K → Ditanya : Suhu akhir (T2) ….? → Jawab : 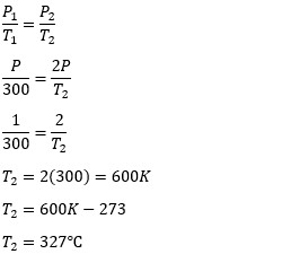 Jadi, suhu akhir didalam bejana tertutup adalah 327°C |
Contoh Soal 4
| 3 mol gas bersuhu 47°C dengan tekanan 2 × 105 Pascal mengalami proses isokhorik hingga tekanan gas bertambah menjadi 3 × 105 Pascal. Perubahan energi dalam gas tersebut adalah …. (Jika, diketahui konstanta gas umum (R) = 8,315 J/mol.K) Pembahasan : → Diketahui : Suhu awal (T1) = 47°C + 273 = 320 K Tekanan awal (P1) = 2 × 105 Pa Tekanan akhir (P2) = 3 × 105 Pa Konstanta gas umum (R) = 8,315 J/mol.K Jumlah mol (n) = 3 → Ditanya : Perubahan energi gas ….? → Jawab : Pada proses isokhorik, gas tidak mengalami perubahan volume, sehingga tidak ada usaha yang dilakukan (W = 0) Hukum I Termodinamika : ΔU = Q – W ΔU = Q – 0 ΔU = Q Dari rumus di atas, disimpulkan bahwa pada proses isokhorik, kalor yang ditambahkan pada sistem (Q) mengakibatkan energi dalam (U) sistem bertambah. Sebaliknya, kalor yang dilepaskan sistem mengakibatkan energi dalam sistem berkurang. Perubahan energi yang terjadi dapat dihitung dengan rumus energi berikut ini. Energi dalam gas : ΔU = 3/2 nR ΔT = 3/2 nR (T2 – T1) Untuk dapat menentukan perubahan energi dalam gas, maka harus diketahui suhu akhir (T2). Nah, untuk menentukan T2, maka dapat digunakan rumus hukum Gay-Lussac berikut ini. Rumus Hukum Gay-Lussac : 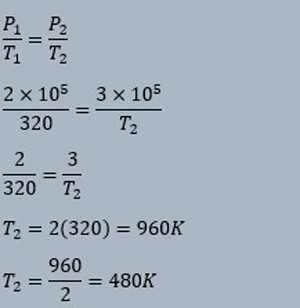 Perhitungan perubahan energi dalam gas : ΔU = 3/2 nR ΔT = 3/2 nR (T2 – T1) ΔU = 3/2 (3)(8,315)(480 – 320) ΔU = 3/2 (3)(8,315)(160) ΔU = 3/2 (3991,2) ΔU = 5986,8 Joule Jadi, perubahan energi dalam gas adalah 5986,8 Joule |
Download Soal Isokhorik PDF
Selain contoh soal di atas, kami juga akan membagikan kisi-kisi dan soal HOST materi termodinamika mulai dari proses isobaric, isothermal, isokhorik dan adiabatic yang bisa kalian download dalam bentuk PDF secara gratis melalui tautan download di bawah ini.
Itulah informasi lengkap yang dapat inspired2write.com sajikan mengenai contoh soal isokhorik dan pembahasannya beserta dengan materi proses isokhorik dalam hukum termodinamika. Mungkin itu saja informasi dari kami, semoga artikel di atas menambah ilmu kalian.